Le système endocannabinoïde représente l’une des découvertes les plus fascinantes de la neurobiologie moderne. Identifié dans les années 1990, ce réseau complexe de molécules de signalisation régule une multitude de processus physiologiques essentiels à notre survie. Les endocannabinoïdes, véritables messagers chimiques produits par notre organisme, orchestrent un ballet moléculaire sophistiqué qui influence notre humeur, notre appétit, notre perception de la douleur et bien d’autres fonctions vitales. Cette machinerie biologique, présente chez tous les mammifères, témoigne de l’importance évolutive de ces mécanismes de régulation. Comprendre le fonctionnement de ce système ouvre des perspectives thérapeutiques prometteuses pour de nombreuses pathologies, de l’épilepsie aux troubles anxieux en passant par les maladies neurodégénératives.
Système endocannabinoïde : architecture moléculaire et distribution tissulaire
Le système endocannabinoïde constitue un réseau de communication intercellulaire d’une complexité remarquable, orchestrant l’homéostasie à travers l’ensemble de l’organisme. Cette architecture moléculaire repose sur trois piliers fondamentaux : les récepteurs cannabinoïdes, les ligands endogènes appelés endocannabinoïdes, et les enzymes responsables de leur synthèse et de leur dégradation. Cette organisation tripartite permet une régulation fine et dynamique des processus physiologiques, adaptant en permanence les réponses cellulaires aux besoins de l’organisme.
Récepteurs CB1 : localisation neuronale et signalisation synaptique
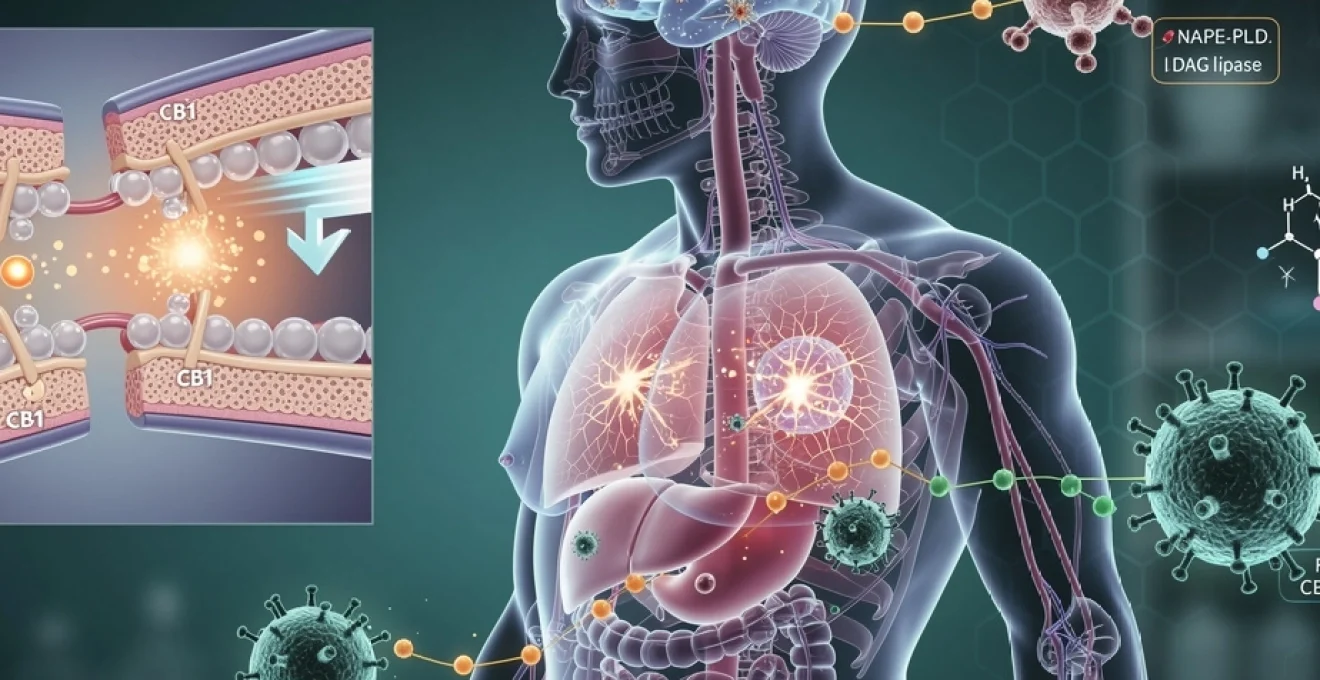
Les récepteurs CB1 représentent les récepteurs couplés aux protéines G les plus abondants du système nerveux central. Leur distribution privilégiée dans l’hippocampe, le cervelet, les ganglions de la base et le cortex cérébral explique leur rôle crucial dans la modulation des fonctions cognitives supérieures. Ces récepteurs exercent principalement une action inhibitrice sur la libération de neurotransmetteurs, agissant comme des modulateurs rétrogrades de la transmission synaptique. Cette localisation stratégique leur confère une influence déterminante sur l’apprentissage, la mémoire, la coordination motrice et les processus émotionnels.
Récepteurs CB2 : expression périphérique et modulation immunitaire
Contrairement aux récepteurs CB1, les récepteurs CB2 présentent une distribution majoritairement périphérique, avec une expression préférentielle dans les cellules du système immunitaire. Les macrophages, les lymphocytes T et B, ainsi que les cellules microgliales constituent les principales populations cellulaires exprimant ces récepteurs. Cette localisation spécifique positionne les récepteurs CB2 comme des régulateurs clés de la réponse inflammatoire et de l’immunité adaptative. Leur activation module la production de cytokines pro-inflammatoires et influence la migration cellulaire lors des processus infectieux ou inflammatoires.
Enzymes de biosynthèse : NAPE-PLD et DAG lipase alpha
La biosynthèse des endocannabinoïdes implique des enzymes hautement spécialisées qui catalysent la formation de ces lipides bioactifs à la demande. La N-arachidonoyl phosphatidyléthanolamine phospholipase D (NAPE-PLD) constitue l’enzyme clé de la synthèse de l’anandamide, hydrolysant son précurseur N-ara
phosphatidyléthanolamine en anandamide. En parallèle, la DAG lipase alpha (DAGLα) catalyse la formation du 2‑arachidonoylglycérol (2‑AG) à partir de diacylglycérols membranaires enrichis en acide arachidonique. Ces enzymes sont étroitement régulées par l’activité neuronale, le taux de calcium intracellulaire et divers neuromodulateurs, ce qui permet une synthèse ultra-localisée et transitoire des endocannabinoïdes. On peut comparer ce mécanisme à un « spray moléculaire » activé uniquement lorsque la cellule dépasse un certain seuil d’excitation, évitant ainsi une stimulation chronique et délétère des récepteurs CB1 et CB2.
Enzymes de dégradation : FAAH et MAGL dans l’homéostasie cannabinoïde
À l’opposé de la biosynthèse, la dégradation rapide des endocannabinoïdes garantit que le signal reste bref et précisément contrôlé. La fatty acid amide hydrolase (FAAH) est l’enzyme principale de catabolisme de l’anandamide et des amides d’acides gras apparentés. Localisée sur les membranes du réticulum endoplasmique et des mitochondries, elle hydrolyse l’anandamide en acide arachidonique et éthanolamine, mettant fin à son action sur les récepteurs CB1 et CB2. De son côté, la monoacylglycérol lipase (MAGL) assure la dégradation du 2‑AG en acide arachidonique et glycérol, principalement dans les terminaisons présynaptiques et les astrocytes.
Ce couple FAAH–MAGL fonctionne comme un véritable « système de freinage moléculaire » du système endocannabinoïde. Lorsque ces enzymes sont inhibées pharmacologiquement, les concentrations locales d’anandamide et de 2‑AG augmentent, amplifiant les effets analgésiques et anti-inflammatoires endogènes. Néanmoins, une inhibition prolongée ou non sélective peut déséquilibrer l’homéostasie lipidique, perturber d’autres voies de signalisation dérivées de l’acide arachidonique et entraîner des effets secondaires. C’est pourquoi les stratégies thérapeutiques actuelles cherchent à cibler de façon tissulaire ou temporaire ces enzymes, plutôt qu’à les bloquer de manière systémique et permanente.
Anandamide : biosynthèse, transport membranaire et mécanismes d’action
L’anandamide, ou N-arachidonoyléthanolamine (AEA), est souvent décrite comme la « molécule de la félicité » en raison de son implication dans la régulation de l’humeur, du stress et de la récompense. Sur le plan biochimique, il s’agit d’un amide d’acide gras dérivé de l’acide arachidonique, produit à la demande dans de nombreux tissus, notamment le cerveau, le tube digestif et le système reproducteur. Sa nature hautement lipophile conditionne à la fois sa synthèse, son transport au sein de la cellule et sa dégradation rapide après action. Pour comprendre son rôle dans le corps humain, il est essentiel de détailler sa voie de biosynthèse, ses mécanismes de transport intracellulaire et sa façon d’interagir avec les récepteurs cannabinoïdes et non cannabinoïdes.
Voie de synthèse via n-arachidonoyl phosphatidyléthanolamine
La principale voie de biosynthèse de l’anandamide repose sur un précurseur membranaire, la N-arachidonoyl phosphatidyléthanolamine (NAPE). Sous l’effet d’augmentations de calcium intracellulaire et de signaux neurotransmetteurs, des phospholipases spécifiques convertissent la NAPE en AEA. L’enzyme la plus caractérisée dans ce processus est la NAPE-PLD, qui hydrolyse directement la NAPE pour libérer l’anandamide. D’autres voies alternatives, impliquant des phospholipases C ou A2 suivies d’amidations, ont également été décrites, soulignant la redondance et la flexibilité de la synthèse d’anandamide dans différentes cellules.
Ce mode de production « à la demande » signifie qu’il n’existe pas de réserves préformées d’anandamide stockées dans des vésicules, contrairement à la sérotonine ou la dopamine. En pratique, cela permet à chaque neurone ou cellule immunitaire d’ajuster finement la production d’AEE en fonction de son état d’activation. Vous pouvez voir cela comme une « cuisine moléculaire minute » : les ingrédients (lipides membranaires) sont toujours disponibles, mais le plat (anandamide) n’est préparé que lorsque la situation physiologique l’exige, par exemple en réponse à un stress aigu ou à un stimulus douloureux.
Protéines de transport intracellulaire : FABP5 et FABP7
Une fois produite dans la membrane plasmique, l’anandamide doit être acheminée vers ses sites d’action ou de dégradation intracellulaires. Compte tenu de sa forte hydrophobicité, ce transport n’est pas laissé au hasard. Des protéines de liaison aux acides gras (FABP), en particulier FABP5 et FABP7, jouent un rôle central comme « navettes » intracellulaires. Elles se lient à l’anandamide et facilitent sa diffusion dans le cytoplasme jusqu’aux compartiments où se trouve la FAAH, principalement au niveau du réticulum endoplasmique et des mitochondries.
Ce système de transport conditionne non seulement la vitesse de dégradation de l’anandamide, mais aussi sa capacité à atteindre certains récepteurs intracellulaires, comme les récepteurs nucléaires PPARα et PPARγ. En modulant l’expression ou l’activité de FABP5 et FABP7, il est donc possible d’influencer indirectement la durée d’action et la portée biologique de l’anandamide dans le système nerveux et les tissus périphériques. Des travaux récents explorent l’inhibition sélective de ces protéines de transport comme stratégie pour renforcer les effets analgésiques et anxiolytiques des endocannabinoïdes, sans recourir à des doses élevées de cannabinoïdes exogènes.
Affinité réceptorielle et modulation de l’AMPc
Sur le plan pharmacologique, l’anandamide agit principalement comme un agoniste partiel des récepteurs CB1 et, à un moindre degré, des récepteurs CB2. Sa forte affinité pour CB1, particulièrement dans le cortex, l’hippocampe et les ganglions de la base, explique son rôle dans la modulation de la neurotransmission glutamatergique et GABAergique. Une fois liée au récepteur CB1, l’anandamide active une protéine G de type Gi/o, ce qui entraîne une inhibition de l’adénylate cyclase et donc une diminution des niveaux intracellulaires d’AMP cyclique (AMPc). Cette réduction de l’AMPc conduit à une baisse de l’activité de la protéine kinase A (PKA) et à la modulation de nombreux canaux ioniques et facteurs de transcription.
Concrètement, cette cascade se traduit par une diminution de la libération de neurotransmetteurs excitateurs (comme le glutamate) ou inhibiteurs (comme le GABA), en fonction du type de neurone ciblé. Cela peut sembler paradoxal, mais ce « réglage fin » permet au système endocannabinoïde de stabiliser l’activité neuronale, un peu comme un régulateur de vitesse corrige en permanence les variations de vitesse d’un véhicule. Par ailleurs, l’anandamide peut activer d’autres cibles, telles que les récepteurs TRPV1 (canaux vanilloïdes) et certains sous-types de récepteurs de la sérotonine, participant à ses effets analgésiques, anxiolytiques et vasodilatateurs.
Dégradation enzymatique par l’amide hydrolase d’acides gras
La fin de vie de l’anandamide est assurée principalement par la fatty acid amide hydrolase (FAAH), une hydrolase située sur les membranes intracellulaires. Après son transport via les FABP, l’anandamide est hydrolysée en acide arachidonique et éthanolamine, deux métabolites qui peuvent être réutilisés dans d’autres voies métaboliques. Cette dégradation rapide explique pourquoi les concentrations basales d’AEE dans le cerveau restent faibles, en dépit d’une synthèse fréquente en réponse aux stimuli physiologiques.
Du point de vue thérapeutique, l’inhibition partielle de la FAAH a été envisagée pour prolonger l’action de l’anandamide, notamment dans la gestion de la douleur chronique ou des troubles anxieux. Toutefois, certains essais cliniques d’inhibiteurs puissants de la FAAH ont mis en évidence des effets indésirables sévères lorsqu’ils étaient administrés à fortes doses et sur de longues périodes. Cela illustre bien le caractère délicat de l’homéostasie endocannabinoïde : soutenir ce système peut être bénéfique, mais le forcer de manière artificielle et durable risque de perturber d’autres circuits de signalisation lipidique étroitement interconnectés.
2-arachidonoylglycérol : métabolisme lipidique et signalisation rétrograde
Le 2‑arachidonoylglycérol (2‑AG) est l’autre pilier majeur des substances endocannabinoïdes dans le corps humain. Quantitativement plus abondant que l’anandamide dans le cerveau, il agit comme un agoniste complet des récepteurs CB1 et CB2, ce qui lui confère une puissance marquée dans la modulation de la transmission synaptique et de la réponse immunitaire. Produit à partir de phospholipides membranaires, le 2‑AG joue un rôle central dans la signalisation rétrograde, particulièrement dans des structures clés comme l’hippocampe. Sa dynamique de synthèse et de dégradation rapide en fait un véritable « messager éclair » de la plasticité synaptique.
Production par hydrolyse du diacylglycérol
La synthèse du 2‑AG débute généralement par l’activation de récepteurs couplés aux protéines G ou de récepteurs tyrosine kinase, qui stimulent la phospholipase Cβ (PLCβ). Cette enzyme clive les phosphoinositides membranaires pour générer du diacylglycérol (DAG), riche en acide arachidonique. Le DAG est ensuite hydrolysé par la DAG lipase alpha (DAGLα) ou, dans certains tissus, par sa variante DAGLβ, pour produire le 2‑AG. Ce processus se déroule principalement au niveau des membranes postsynaptiques, en réponse à une élévation du calcium intracellulaire et à une activation soutenue des synapses.
Du fait de cette organisation spatiale, la production de 2‑AG est fortement couplée à l’activité neuronale locale. Plus une synapse est sollicitée, plus la cellule postsynaptique est susceptible de générer du 2‑AG pour rétrocontrôler la libération de neurotransmetteurs. On peut comparer ce mécanisme à un système de « feedback automatique » dans un amplificateur audio : lorsque le volume monte trop haut, un signal est renvoyé à la source pour réduire l’intensité et éviter la saturation. C’est précisément ce rôle de régulation que joue le 2‑AG dans de nombreuses microcircuits neuronaux.
Signalisation synaptique rétrograde dans l’hippocampe
L’hippocampe constitue l’un des modèles les plus étudiés pour comprendre la signalisation rétrograde du 2‑AG. Lors d’une stimulation intense des neurones pyramidaux, l’augmentation de calcium dans la cellule postsynaptique déclenche la synthèse de 2‑AG à partir des DAG. Le 2‑AG diffuse ensuite à travers la fente synaptique pour se lier aux récepteurs CB1 situés sur la terminaison présynaptique, qu’elle soit GABAergique ou glutamatergique. Cette activation des CB1 réduit la probabilité de libération de vésicules de neurotransmetteurs, diminuant ainsi la force de la transmission synaptique.
Ce mécanisme est au cœur de phénomènes tels que la dépression synaptique à court terme et la dépolarisation induite de l’inhibition (DSI) ou de l’excitation (DSE). En modulant la quantité de GABA ou de glutamate libérée, le 2‑AG contribue à ajuster la balance excitation–inhibition dans les réseaux hippocampiques, élément fondamental pour la formation de la mémoire et la prévention de l’hyperexcitabilité, notamment dans les contextes épileptiques. Pour vous, cela signifie que les variations fines de 2‑AG peuvent influencer, à un niveau très concret, la capacité à encoder de nouveaux souvenirs ou à résister aux crises.
Métabolisme par la monoacylglycérol lipase
Comme pour l’anandamide, l’action du 2‑AG est strictement limitée dans le temps par un catabolisme enzymatique efficace. La monoacylglycérol lipase (MAGL) est l’enzyme principale de dégradation du 2‑AG dans le cerveau, localisée en grande partie dans les terminaisons présynaptiques. Elle hydrolyse rapidement le 2‑AG en acide arachidonique et glycérol, permettant au neurone de réinitialiser son état basal. D’autres hydrolases, comme ABHD6 et ABHD12, participent également au catabolisme du 2‑AG dans certains compartiments cellulaires, notamment les microglies et les cellules postsynaptiques.
Le contrôle précis de la MAGL est crucial pour éviter l’accumulation excessive de 2‑AG, qui pourrait entraîner une désensibilisation des récepteurs CB1 et perturber d’autres voies de signalisation de l’acide arachidonique, notamment la synthèse des eicosanoïdes pro-inflammatoires. Des inhibiteurs sélectifs de la MAGL sont actuellement étudiés comme outils pharmacologiques pour augmenter transitoirement le tonus endocannabinoïde dans des troubles comme la douleur neuropathique ou l’anxiété. Là encore, l’enjeu consiste à trouver un compromis entre un effet thérapeutique notable et le maintien de l’homéostasie lipidique globale.
Régulation de la plasticité synaptique à long terme
Au-delà des effets à court terme, le 2‑AG participe à la plasticité synaptique à long terme, c’est-à-dire à la capacité durable des synapses à renforcer ou affaiblir leur efficacité. Dans plusieurs régions du cerveau, dont l’hippocampe et les ganglions de la base, l’activation répétée des récepteurs CB1 par le 2‑AG peut induire une diminution à long terme (LTD) de la libération de neurotransmetteurs. Cette LTD dépendante des CB1 modifie durablement les circuits neuronaux, influençant des fonctions telles que l’apprentissage moteur, la mémoire émotionnelle et les comportements de récompense.
Par exemple, dans le striatum, la LTD médiée par le 2‑AG joue un rôle important dans l’adaptation aux habitudes et dans la réponse aux drogues addictives. Une altération de cette composante endocannabinoïde de la plasticité synaptique est observée dans des pathologies comme la maladie de Parkinson, la dépendance ou certains troubles anxieux. Comprendre ces mécanismes ouvre la voie à des interventions thérapeutiques ciblées, cherchant non seulement à soulager les symptômes, mais aussi à recalibrer les circuits neuronaux sous-jacents.
Régulation neuroendocrine par les endocannabinoïdes hypothalamiques
L’hypothalamus est un centre de commande majeur de l’axe neuroendocrinien, chargé de coordonner la faim, la soif, la température corporelle, le rythme circadien et les réponses au stress. Les substances endocannabinoïdes y occupent une place stratégique en modulant la libération de nombreux neuropeptides et hormones hypophysaires. Les récepteurs CB1 sont abondamment exprimés dans des noyaux hypothalamiques clés, tels que le noyau arqué, le noyau paraventriculaire et l’aire hypothalamique latérale, où ils contrôlent l’activité de neurones produisant la ghréline, la leptine, la CRH ou encore la GnRH.
Sur le plan métabolique, l’activation des CB1 hypothalamiques favorise la prise alimentaire et le stockage énergétique, en augmentant la sensation de faim et en modulant les circuits de récompense associés à l’alimentation. Inversement, un tonus endocannabinoïde réduit est associé à une diminution de l’appétit et à une meilleure sensibilité à l’insuline. C’est ce principe qui avait inspiré le développement d’antagonistes des CB1, comme le rimonabant, pour traiter l’obésité et le syndrome métabolique. Toutefois, en bloquant également les CB1 cérébraux impliqués dans la régulation de l’humeur, ces traitements se sont révélés anxiogènes et dépressogènes, illustrant la délicate interdépendance entre métabolisme et santé mentale.
Les endocannabinoïdes hypothalamiques interviennent aussi dans la régulation de l’axe hypothalamo–hypophyso–surrénalien (HHS), qui gère la réponse au stress. En condition aiguë, une augmentation transitoire d’anandamide et de 2‑AG contribue à limiter la production de CRH et de cortisol, favorisant un retour à l’équilibre une fois la menace passée. En revanche, un dysfonctionnement chronique de ce contrôle endocannabinoïde peut participer à l’installation de troubles anxieux, d’épisodes dépressifs ou de perturbations du sommeil. Pour vous, cela signifie que soutenir, par le mode de vie (sommeil, alimentation, gestion du stress), un fonctionnement optimal de ce système pourrait aider à mieux amortir les chocs du quotidien.
Modulation immunitaire et réponse inflammatoire via les récepteurs CB2
Au niveau du système immunitaire, les substances endocannabinoïdes jouent un rôle de chefs d’orchestre discrets en modulant l’intensité et la durée de la réponse inflammatoire. Les récepteurs CB2, largement exprimés sur les lymphocytes, macrophages, cellules dendritiques et microglies, sont la principale interface entre le système endocannabinoïde et l’immunité. L’activation de ces récepteurs par le 2‑AG, l’anandamide ou des médiateurs endocannabinoïdes-like (comme le PEA) influence la production de cytokines, la prolifération cellulaire et la migration vers les sites d’inflammation.
De nombreuses études montrent que la stimulation des CB2 tend à réduire la production de cytokines pro-inflammatoires (TNF-α, IL‑1β, IL‑6) tout en favorisant des profils plus régulateurs ou anti-inflammatoires (IL‑10, TGF‑β). Cette action permet de limiter les dommages tissulaires lors des infections, des traumatismes ou des maladies auto-immunes. Par analogie, on peut considérer les endocannabinoïdes comme un « thermostat immunitaire » : lorsqu’une réponse est nécessaire, ils la laissent s’exprimer, mais ils contribuent ensuite à abaisser progressivement le niveau d’alerte pour prévenir l’emballement et la chronicisation de l’inflammation.
Sur le plan clinique, des altérations de la signalisation via les CB2 ont été décrites dans des pathologies telles que la polyarthrite rhumatoïde, la sclérose en plaques, les maladies inflammatoires chroniques de l’intestin ou encore certaines formes d’asthme. Des agonistes sélectifs de CB2 et des modulateurs du tonus endocannabinoïde sont activement explorés comme stratégies pour réduire l’inflammation chronique tout en préservant la capacité de l’organisme à se défendre contre les agents infectieux. Pour les personnes concernées, cela pourrait, à terme, se traduire par des traitements plus ciblés, associés à moins d’effets immunosuppresseurs généralisés que les thérapies actuelles.
Pathologies associées aux dysfonctionnements du système endocannabinoïde
Compte tenu de son omniprésence dans le cerveau, le système immunitaire, le métabolisme et la régulation hormonale, il n’est pas surprenant que des altérations du système endocannabinoïde soient impliquées dans de nombreuses pathologies humaines. Les déséquilibres peuvent prendre plusieurs formes : diminution ou augmentation anormale des niveaux d’anandamide ou de 2‑AG, expression modifiée des récepteurs CB1/CB2, activité altérée des enzymes de synthèse ou de dégradation, ou encore perturbation des protéines de transport. Ces dérégulations ont été observées dans des maladies neurologiques (épilepsie, maladie d’Alzheimer, maladie de Parkinson), psychiatriques (dépression, troubles anxieux, addiction), métaboliques (obésité, diabète de type 2), inflammatoires et auto-immunes, ainsi que dans certains cancers.
Par exemple, dans l’obésité et les syndromes métaboliques, un hyperfonctionnement du tonus endocannabinoïde périphérique favorise la lipogenèse, l’insulinorésistance et la prise de poids, tandis qu’au niveau cérébral, un dérèglement des CB1 contribue à l’hyperphagie et à la recherche accrue de récompense alimentaire. À l’inverse, dans certaines dépressions majeures ou troubles de stress post-traumatique, on observe une diminution des niveaux d’anandamide et une altération de la signalisation CB1 dans des régions clés de la régulation émotionnelle. Cette « carence endocannabinoïde » pourrait expliquer une partie de la vulnérabilité au stress et des difficultés à retrouver un état d’équilibre émotionnel après un traumatisme.
Dans le domaine de la douleur chronique, des anomalies de la signalisation endocannabinoïde ont été mises en évidence tant au niveau central que périphérique, ouvrant la voie à des approches visant à renforcer ce système pour réduire la nociception. Enfin, dans plusieurs cancers, les récepteurs CB1, CB2 et certaines enzymes comme la MAGL sont surexprimés ou dérégulés, et les endocannabinoïdes peuvent influencer la prolifération, l’angiogenèse et la migration des cellules tumorales. Cette complexité explique pourquoi, malgré un potentiel considérable, la modulation thérapeutique du système endocannabinoïde doit être envisagée avec nuance, en tenant compte du contexte tissulaire, du stade de la maladie et des interactions avec d’autres systèmes de signalisation.